Le projet de DeReM-SE
Cancer
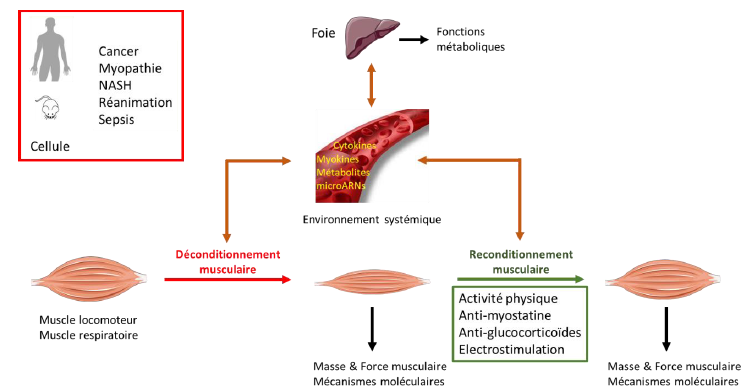
La cachexie est une forme de déconditionnement musculaire extrêmement rapide et sévère (quelques jours à quelques mois) dont la prévalence est particulièrement élevée dans les cancers (Teunissen et al. 2007). De plus, les différentes interventions thérapeutiques (exérèse, chimiothérapie, radiothérapie) peuvent exacerber ce déconditionnement musculaire. Les mécanismes de régulation de la masse musculaire squelettique au cours de la cachexie associée au cancer sont maintenant relativement bien compris (Argiles et al. 2014). Des travaux antérieurs de l’équipe ont notamment mis en évidence l'existence d'un déséquilibre entre la synthèse et la dégradation des protéines musculaires (Gallot et al. 2014). En revanche, les régulateurs extrinsèques à l'origine de l'activation de ce programme catabolique sont mal connus. Le rôle des glucocorticoïdes comme facteurs extrinsèques contribuant à la cachexie associée au cancer sera étudié chez la souris ApcMin/+, un modèle murin de cancer de l’intestin grêle et du côlon (collaboration Équipe ATPA LIBM). Les effets systémiques du déconditionnement musculaire seront étudiés en lien avec la régulation du métabolisme hépatique. En effet, le tissu musculaire est un partenaire métabolique privilégié du tissu hépatique, des altérations du fonctionnement musculaire pouvant altérer le fonctionnement hépatique, et réciproquement (Argiles et al. 2018).
Des travaux de l’équipe avaient montré que l’inhibition du gène de la myostatine, un régulateur négatif de la masse musculaire (Durieux et al. 2007), était une stratégie efficace pour prévenir la cachexie chez la souris ApcMin/+ (Gallot et al. 2014). Les effets systémiques de la prévention de la cachexie musculaire par invalidation du gène de la myostatine seront également déterminés en lien avec la régulation du métabolisme hépatique. L’importance fonctionnelle que peuvent avoir les glucocorticoïdes dans ce contexte sera également appréhendée (collaboration Équipe ATPA LIBM). Les effets du déconditionnement musculaire sur la récupération à moyen terme seront également explorés dans le cadre de l’étude clinique MYOCAC (ClinicalTrials Identifier NCT03172403) chez une population de patients atteints de cancers de l’estomac, de l’intestin grêle, de l’appendice, du côlon, et du rectum. L’analyse biologique de la biopsie musculaire obtenue lors de la résection chirurgicale sera couplée à une analyse du capital musculaire, à une analyse fonctionnelle musculaire et à une analyse biologique de l’environnement systémique jusqu’à 6 mois après l’intervention chirurgicale (collaborations Équipe ATPA LIBM, Équipe PAF LIBM).
Déconditionnement musculaire en anesthésie-réanimation
Le déconditionnement musculaire acquis en unité de soins intensifs est une complication fréquente à des maladies graves associée à une mortalité et une morbidité élevée, le sepsis étant une condition aggravante de ce déconditionnement (Griffiths et Hall 2010). Des travaux antérieurs de l’équipe ont bien décrit les mécanismes mis en jeu dans le déconditionnement et au cours de la récupération dans un modèle murin de sepsis (Morel et al. 2017). Cependant, les régulateurs extrinsèques à l'origine de l'activation de ce programme catabolique sont encore mal connus. Le rôle des glucocorticoïdes dans le déconditionnement musculaire sera déterminé lors du sepsis. Les effets de l’invalidation du gène de la myostatine seront également étudiés dans ce contexte.
Le diagnostic précoce du déconditionnement musculaire du patient en service de réanimation est une donnée importante pour le clinicien puisqu’elle va lui permettre d’orienter et d’adapter sa pratique thérapeutique. L’analyse du déconditionnement musculaire au lit du patient (morphométrie et force musculaires, environnement systémique) permettra de développer des techniques de réhabilitation innovantes et adaptées (électrostimulation musculaire, cycloergomètre) avec pour objectif d’améliorer la qualité de soins, le pronostic et la qualité de vie post-réanimation des patients (collaboration Équipe PAF LIBM).
Le déconditionnement musculaire acquis en unité de soins intensifs touche aussi les muscles respiratoires. Si nos travaux conduits chez l’animal ont mis en évidence une résistance catabolique des muscles respiratoires comparativement aux muscles locomoteurs (Morel et al. 2017), la situation est tout à fait différente en clinique chez l’humain. En effet, la ventilation mécanique qui permet de suppléer la fonction ventilatoire parfois pendant une période prolongée chez les patients septiques peut devenir un acteur majeur du déconditionnement des muscles respiratoires (Levine et al. 2008). L’étude SEPTIC (ClinicalTrials Identifier NCT03371602) a pour objet l’étude de l'impact combiné de la ventilation mécanique et du sepsis sur le diaphragme humain. Les mécanismes moléculaires du déconditionnement musculaire seront explorés dans le muscle diaphragme de patients contrôles (chirurgie abdominale ou thoracique programmée non septique sus-mésocolique : gastrectomie, oesophagectomie, pancréatectomie, hépatectomie), de patients septiques (chirurgie abdominale ou thoracique dans un contexte septique : péritonite, médiastinite, abcès pleural), de patients ventilés en mort encéphalique pour lequel un prélèvement multi organe est prévu, et de patients sous ventilation mécanique contrôlée devant être opérés d’une chirurgie abdominale ou thoracique dans un contexte septique.
La pré-habilitation est une modalité de prise en charge pré-opératoire des patients ayant une chirurgie lourde programmée dont la finalité est de réduire les complications post-opératoires et donc la durée de séjour en service de réanimation. Afin de caractériser les patients à risque nécessitant une pré-thérapeutique, le capital musculaire, la biologie musculaire, l’environnement systémique et le niveau d’activité physique de patients de chirurgie cardiaque seront déterminés en pré-opératoire et associés au devenir du patient jusqu’à 6 mois post-opératoire.
Stéatose hépatique
Le foie et le tissu musculaire sont des partenaires métaboliques privilégiés via la régulation des métabolismes du glucose, des lipides ou des acides aminés, mais aussi via les interactions cytokiniques. Cette relation entre ces 2 tissus a déjà été abordée dans le contexte des effets du déconditionnement musculaire associé au cancer et au sepsis. Ici, seront envisagés les effets de la pathologie hépatique sur le tissu musculaire. La stéatohépatite non alcoolique (NASH, pour nonalcoholic steatohepatitis) est caractérisée par une accumulation excessive de triglycérides dans le foie associée à un état inflammatoire marqué (De Bandt 2018). Si les patients atteints de NASH font l’expérience d’un déconditionnement musculaire (De Bandt 2018), les effets de cet état inflammatoire sur le tissu musculaire ne sont actuellement pas connus. L’utilisation de modèles de co-culture primaire hépatocytes-myotubes permettra de déterminer les effets de l’environnement, modulé par l’hépatocyte, sur le tissu musculaire.
Myopathie congénitale
Contrairement aux pathologies précédentes pour lesquelles le déconditionnement survenait en réponse à l’évolution d’une pathologie d’origine non musculaire, les myopathies congénitales ont une origine et une expression essentiellement musculaire. La myopathie centronucléaire liée à la mutation du gène dynamine 2 (dnm2) est une pathologie caractérisée par un déconditionnement musculaire dont la manifestation pourra être plus ou moins précoce (de l’enfance à l’âge adulte). La souris KI dnm2 est le modèle murin de cette pathologie (Durieux 2012). Les effets de l’invalidation du gène de la myostatine sur le déconditionnement musculaire de la souris KI dnm2, (Durieux et al. 2012) seront déterminés. Par ailleurs, des données préliminaires de l’équipe ont permis de mettre en évidence l’existence d’anomalies structurales témoignant probablement d’une dérégulation de l’homéostasie mitochondriale dans les fibres musculaires des souris KI dnm2. Ce travail sera poursuivi par l’analyse du métabolisme mitochondrial et des mécanismes de fusion et de fission mitochondriale. Les effets d’un entrainement à l’endurance sur l’homéostasie mitochondriale et l’amélioration du phénotype musculaire des souris KI dnm2 seront également déterminés.

 Lyon - Saint-Etienne - Chambéry
Lyon - Saint-Etienne - Chambéry