Le Projet de VBRBC
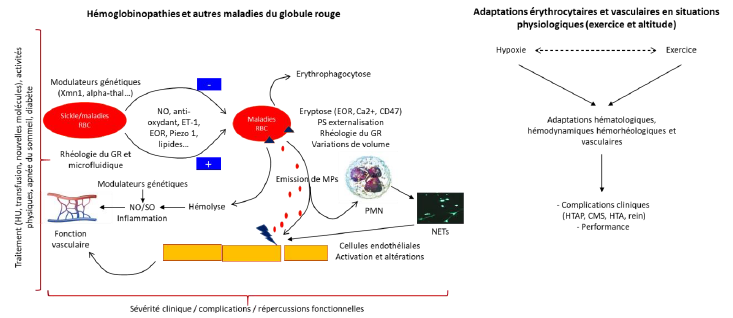
1. Hémoglobinopathies et autres maladies du globule rouge
1.1. Rhéologie du sang, génétique, et microcirculation
Comme lors du précédent contrat (Connes et al. 2016 ; Renoux et al. 2016 ; 2017 ; 2019 ; Ballas et al. 2018), le travail sur l’implication des anomalies de la rhéologie du sang et des gènes modificateurs dans la physiopathologie de la drépanocytose sera poursuivi. Il est envisagé notamment d’étudier les propriétés de déformabilité érythrocytaire par ektacytométrie en gradient d’oxygène pour déterminer la pression partielle en oxygène critique de falciformation (POS : point of sickling) (Rab et al. 2018). La mesure de ce POS pourrait devenir un marqueur biologique à valeur -pronostique dans le suivi des patients drépanocytaires. Nous testerons également les associations entre ce POS et la sévérité clinique (complications vaso-occlusives et hémolytiques). Cette mesure sera également confrontée à différents modulateurs génétiques de la drépanocytose. Les modulateurs traditionnels (alpha-thalassémie, déficit en G6PD, haplotypes β-globine) sont déjà génotypés en routine depuis plusieurs années dans notre équipe par séquençage Sanger, gap-PCR multiplex, HRM et FRET. Pour aller plus loin, l’étude de l’influence des gènes modificateurs sera étendue à d’autres gènes (NOS1 et 2, APOL1, CD36, gènes du stress-oxydant, VCAM1, etc). Ce panel d’une soixantaine de gènes permettra de tester de nouvelles associations phénotype-génotype et de confirmer certaines d’entre elles jamais répliquées dans la littérature. Enfin, seront étudiés les effets de différents traitements sur le POS : hydroxyurée, transfusion sanguine et molécules à potentiel thérapeutique.
Dans le but de mieux comprendre l’impact des anomalies de la rhéologie sanguine sur la microcirculation, un certain nombre d’études dans le champ de la microfluidique seront conduites. Un système microfluidique particulier sera utilisé afin d’étudier le temps de transit des globules rouges de différentes pathologies dans des capillaires dimensionnés et le temps mis par ces globules rouges pour récupérer leur forme de repos après déformation (élasticité membranaire). Par ailleurs, en raison de leurs propriétés d’agrégation différentes, nous évaluerons la capacité des globules rouges de patients et de sujets sains à former des clusters d’agrégats hydrodynamiques dans des capillaires de quelques µm. Ce phénomène pourrait avoir une forte implication clinique car la formation de cluster d’agrégats hydrodynamiques est susceptible d’altérer le flux sanguin dans la microcirculation. Le flux microcirculatoire in-vivo au niveau sublingual (système Microvision) chez des patients drépanocytaires sera également étudié et les associations avec le niveau de déformabilité et d’agrégation érythrocytaire seront testées.
1.2. Eryptose, microparticules et fonction vasculaire dans la drépanocytose et la sphérocytose héréditaire
Durant les 2 dernières décennies, l’idée de la présence d’une vasculopathie chronique dans la drépanocytose s’est imposée. Le stress oxydatif majoré, la diminution de la biodisponibilité en monoxyde d’azote et la présence de quantités importantes de microparticules dans le plasma sont autant de facteurs pouvant contribuer à l’apparition de cette vasculopathie (Charlot et al. 2016 ; Moeckesch et al. 2017).
Le projet VASCU-DREPA aura pour objectif de tester les facteurs biologiques (inflammation, stress oxydatif, microparticules) responsables de la dysfonction micro-vasculaire et macro-vasculaire chez des patients drépanocytaires adultes. Puisque l’activité physique régulière module la fonction vasculaire chez le sujet sain, nous explorerons également la relation entre le niveau d’activité physique et le degré de dysfonction vasculaire chez le drépanocytaire. Par ailleurs, le syndrome d’apnées obstructives du sommeil est impliqué dans la dysfonction vasculaire observée chez les patients obèses. Le projet DREPA-APNEE permettra de tester les effets de l’apnée du sommeil et d’une hypoxémie nocturne sur la sévérité clinique, la fonction vasculaire et ses déterminants biologiques chez les patients drépanocytaires enfants et adultes à Lyon. Enfin, il semble important de caractériser le niveau d’éryptose dans la sphérocytose héréditaire (patients splénectomisés et non-splénectomisés) et tester les associations avec la fonction vasculaire puisqu’il a été montré que les patients splénectomisés avaient un risque accru de développer des vasculopathies (Crary et al. 2011).
Durant le précédent contrat, nous avons commencé à tester les effets de différentes molécules (donneurs de monoxyde d’azote, anti-oxydants et oxydants) sur les propriétés rhéologiques du globule rouge et les marqueurs d’éryptose dans la drépanocytose. Les premiers résultats ont montré une éryptose avancée dans la drépanocytose (quantité d’espèces réactives de l’oxygène, de phosphatidylsérine externalisée et de calcium intra-érythrocytaire plus importantes chez les patients drépanocytaires que chez des sujets sains), ainsi qu’un nombre de microparticules circulantes d’origine érythrocytaire plus élevé. Il est envisagé de tester les effets potentiellement délétères de ces microparticules érythrocytaires drépanocytaires sur l’intégrité et le phénotype des cellules endothéliales. La voie des Toll Like Receptor 4 (TLR4) et la voie de la phosphatidylserine. Nous testerons également les effets de l’éryptose avancée de globules rouges drépanocytaires sur l’activité erythro-phagocytaire seront explorées. Enfin, des travaux récents ont identifié une protéine mécano-sensible, la protéine Piezo-1, capable de faire rentrer du calcium dans les globules rouges et qui pourrait ainsi moduler le degré de déshydratation cellulaire, l’éryptose et les anomalies rhéologiques du globule rouge dans différentes pathologies érythrocytaires (Brugnara, 2018). Nous étudierons les effets d’une modulation de l’activité Piezo-1 sur ces paramètres dans la drépanocytose ainsi que le degré d’activation de la voie Gardos et de l’échangeur K-Cl.
1.3. Activité physique et drépanocytose
Comme dans beaucoup de pathologies chroniques, les patients drépanocytaires ont une aptitude physique générale réduite par rapport à la population générale. Le principal facteur incriminé est l’anémie. Mais de récentes études réalisées par l’équipe PAF du LIBM ont également rapporté des anomalies structurales et énergétiques, ainsi qu’un remodelage microvasculaire, dans le muscle des patients drépanocytaires (Ravelojaona et al. 2015). Les répercussions fonctionnelles de ces anomalies chez le drépanocytaire seront donc étudiées au travers d’une étude qui décryptera le comportement électromyographique et l’oxygénation musculaire au cours d’un exercice d’endurance musculaire localisé et d’un test de marche (étude DREPA-MUSCLE). Cette étude sera réalisée en collaboration avec l’équipe SPIP du LIBM. En parallèle, des séances d’activité physique adaptée chez le drépanocytaire seront mises en place afin d’en évaluer l’impact clinique, physiologique, biologique et sur la qualité de vie (collaborations avec le service EFR de la Croix Rousse / Service de Médecine du Sport Pédiatrique à l’Hôpital Femme-Mère-Enfant).
1.4. Trait drépanocytaire et diabète de type 2
Lors du précédent contrat, nous avons démontré que la présence du trait drépanocytaire majorait la dysfonction vasculaire et augmentait le risque de complications vasculaires (rétinopathie, hypertension artérielle, glomérulopathie) chez des patients diabétiques de type 2 (Diaw et al. 2015 ; Skinner et al. 2018). Nous avons identifié une implication des produits de fin de glycation (AGEs) dans cette dysfonction vasculaire plus marquée. Pour essayer d’aller plus loin dans les causes de cette dysfonction vasculaire plus marquée, une approche métabolomique est envisagée. Par ailleurs, nous avons démontré dans le précédent contrat (collaboration avec l’UMR 5305 CNRS Lyon, Drs B Fromy et D Sigaudo-Roussel) une dysfonction vasculaire marquée dans un modèle de souris porteuses du trait drépanocytaire (souris Townes hétérozygotes) rendus diabétiques (régime gras et sucré). Nous avons observé une vasodilation induite par la pression (PIV) réduite chez ces souris (Skinner et al. 2019). En revanche, nous avons également observé de façon surprenante une vasodilatation plus marquée en réponse à l’Acétylcholine (AcH). Pour mieux comprendre les causes de cette observation, nous étudierons la voie COX-2 qui, de par l’inflammation générée, pourrait provoquer une vasodilatation transitoire à l’AcH accrue.
2. Exercice/hypoxie
Durant le précédent contrat, nous avons également réalisé plusieurs études dans le domaine des réponses érythrocytaires et vasculaires à l’exercice et/ou les conséquences d’une exposition à l’altitude. Sur le plan hématologique, ces situations physiologiques conduisent à observer l’opposé de ce qui est observé dans la drépanocytose ou d’autres maladies du globule rouge (polyglobulie versus anémie). Malgré cela, il existe beaucoup de points communs : a) l’hyperleucocytose d’exercice et l’hyperleucocytose dans la drépanocytose, b) l’hyperviscosité sanguine d’exercice, l’hyperviscosité sanguine chez les polyglobuliques et l’hyperviscosité sanguine chez les drépanocytaires, c) la présence de vaisseaux quasiment dilatés au maximum chez les natifs de haute altitude et les drépanocytaires, d) la perte de vaso-réactivité chez les natifs d’altitude versus les drépanocytaires. Par ailleurs, certains athlètes peuvent développer une hypoxémie induite par l’exercice, les natifs d’altitude sont exposés de façon chronique à l’hypoxie et les drépanocytaires, de part la présence d’une anémie, sont également exposés à un stress hypoxique. L’hypoxie semble donc constituer un dénominateur commun entre ces différentes situations mais les conséquences sont extrêmement différentes. Comprendre les relations entre les modifications hématologiques, hémorhéologiques et les réponses vasculaires dans chacune de ces situations permettra de mieux comprendre les mécanismes physiologiques/physiopathologiques conduisant à un certain nombre de complications cliniques aiguës et chroniques.
Nous avons très largement décrit les réponses hématologiques et hémorhéologiques lors d’un exercice aigu par le passé (Connes et al. 2013 ; Simmonds et al. 2013). Généralement, au cours d’un effort sur cyclo-ergomètre, on observe une augmentation de la viscosité sanguine, principalement liée à une augmentation de l’hématocrite. Alors que cette augmentation de la viscosité sanguine à l’effort était interprétée par le passé comme quelque chose pouvant être contraignant pour le système cardiovasculaire (augmentation de la post-charge cardiaque), il semblerait aussi qu’elle soit propice à la vasodilatation d’exercice, en tout cas chez le sujet sain. Néanmoins, il a été montré que les athlètes d’endurance qui avaient la plus grosse augmentation de la viscosité sanguine à l’effort développaient aussi une hypoxémie induite par l’exercice (HIE). La présence d’une HIE semble moduler la performance aérobie au niveau de la mer. Cette HIE étant exacerbée en altitude, nous testerons l'impact d’une exposition aigue et chronique à l’hypoxie (moyenne altitude : 2200 m) sur le profil hémorhéologique des athlètes entraînés en endurance et évaluerons les conséquences sur l’hémodynamique pulmonaire et le degré de sévérité de l’HIE.
De façon surprenante, très peu d’études ont été réalisées en course à pied. Dans une étude récente, nous avons observé une augmentation de l’hématocrite lors d’un test progressif et maximal réalisé sur cyclo-ergomètre ou sur tapis roulant mais aucun changement de la viscosité sanguine dans le deuxième cas (Nader et al. 2018). L’augmentation de la déformabilité érythrocytaire observée sur tapis a permis de compenser les effets de l’augmentation de l’hématocrite sur la viscosité sanguine. Ces observations sont surprenantes et les causes non élucidées. Ainsi, nous testerons les effets de plusieurs types d’effort sur les modifications hémorhéologiques et érythrocytaires (électrophysiologie érythrocytaire, marqueurs d’éryptose, d’hydratation érythrocytaire et d’hémolyse). Trois projets sont en cours d’élaboration : 1) effets d’un 10 km en course à pied, 2) effets d’un exercice sur vélo de 40 min au-dessus du seuil ventilatoire, 3) effets de trails de différentes durées. Le 3ème projet sera réalisé pendant la semaine de l’Ultra-Trail du Mont-Blanc (UTMB) en collaboration avec les équipes PAF et SPIP du LIBM. Nous explorerons différents marqueurs érythrocytaires, hématologiques et biochimiques, en lien avec le niveau de déshydratation et la performance. Il a également été proposé qu’une déshydratation trop marquée pourrait augmenter le risque de dysfonction rénale post-effort pouvant même aller jusqu’à l’insuffisance rénale. Nous explorerons donc également les associations entre ces marqueurs biologiques, le niveau de déshydratation et la fonction rénale.
Enfin, plusieurs membres de notre équipe ont été impliqués dans le projet EXPEDITION 5300 : http://expedition5300.com Il a porté sur les mécanismes impliqués dans le mal chronique des montagnes (CMS) et l’hypertension artérielle pulmonaire (HTAP). Ce projet a été une première mondiale et a été très médiatisé, notamment car il s’est déroulé dans la ville la plus haute du monde : La Rinconada, Pérou, 5300 m. Les premiers résultats semblent montrer une implication majeure de l’hyperviscosité sanguine dans le CMS (mais pas dans l’HTAP). Les analyses sur les fonctions macrovasculaires, microvasculaires et cardiaques sont en cours. Nous avons également réalisé plusieurs prélèvements de plasma et il reste maintenant à analyser les marqueurs de l’inflammation, de l’activation endothéliale et du stress oxydatif. Une fois toutes ces analyses réalisées, nous testerons les effets du plasma sur le phénotype de cellules endothéliales de la macrocirculation (expression de VCAM-1, ICAM-1 et des sélectines). Les conclusions de cette expédition permettront de définir les objectifs de la prochaine expédition prévue dans 2 ans.

 Lyon - Saint-Etienne - Chambéry
Lyon - Saint-Etienne - Chambéry